دانلود جزوه ترمودینامیک 1 | 20 میشم
دانلود جزوه ترمودینامیک 1 | 20 میشم


دانلود جزوه ترمودینامیک 1 | 20 میشم
فایل مورد نظردر قالب pdf با حجم 5.87 مگابایت می باشد. دوستان گرامی و دانش آموزان ارجمند و عزیز در صورت تمایل می توانید این فایل بسیار با ارزش را به صورت مستقیم از سایت بیست میشم تهیه بفرمائید.
دانلود جزوه ترمودینامیک 1 | 20 میشم
دانلود جزوه کامل درس ترمودینامیک
ترمودینامیک
دانلود جزوه ترمودینامیک 1 | 20 میشم بیان میدارد ترمودینامیک علم مطالعه گرما و انرژی است.
در دل این علم، قوانینی وجود دارند که میتوانند نحوه انتقال انرژی در اتمها، گردبادها و حتی سیاهچالهها را توصیف کنند.
قانون اول ترمودینامیک توضیح میدهد که چرا انرژی نمیتواند به وجود بیاید یا از بین برود. همچنین این قانون، تبدیل شدن انرژی به شکلهای مختلف را توضیح میدهد.
این در حالی است که قانون دوم ترمودینامیک، مسیر اتفاق افتادن یک فرآیند را پیشبینی میکند. قانون دوم، مکانیزم کارکرد کیهان را به ما نشان میدهد و یادآوری میکند که روزی دنیا به پایان خواهد رسید.
دانلود جزوه ترمودینامیک 1 | 20 میشم
انتقال انرژی
انرژی، قابلیت انجام کار است. انرژیهای یک سیستم، شامل انرژی پتانسیل، درونی و جنبشی هستند. تغییرات انرژی یک سیستم را میتوان به صورت زیر بیان کرد:
![]()
در این معادله تغییرات انرژی پتانسیل، جنبشی و درونی، به ترتیب برابر هستند با:
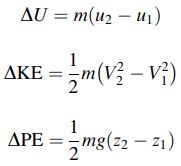
در اکثر مسائل مهندسی، تغییرات انرژی جنبشی و پتانسیل وجود ندارند. با این فرض میتوان تغییرات انرژی سیستم را به صورت زیر بیان کرد:
![]()
در بسیاری از متون علمی، پارامتری که مورد بررسی قرار میگیرد انرژی بر واحد جرم است که معادل است با:
![]()
دانلود جزوه ترمودینامیک 1 | 20 میشم
انتقال جرم
هر جرمی که به درون سیستمی وارد میشود، حامل انرژی است. بنابراین در هنگام وارد شدن تودهای از جرم به یک سیستم، انرژی آن افزایش و در هنگام خارج شدن از آن، انرژی سیستم کاهش مییابد. زمانی که جرمی با نرخ m به یک سیستم وارد میشود، نرخ انرژی وارد شده به آن برابر است با:
![]()
در این معادله h=u+pv است و pv، کار جریان نامیده میشود. در ادامه در مورد اجزا تشکیل دهنده این معادله بیشتر صحبت خواهیم کرد.
دانلود جزوه ترمودینامیک 1 | 20 میشم
دانلود جزوه کامل درس ترمودینامیک
انتقال حرارت
«جیمز ژول» (James Joul)، برای اولین بار و با استفاده از آزمایش، نشان داد که انرژی، این قابلیت را دارد که به شکلهای مختلفی تبدیل شود.
گرما، شکلی از انرژی است و انتقال حرارت نیز زمانی اتفاق میافتد که در یک محیط جامد و یا سیال، اختلاف دمایی وجود داشته باشد.
واحد انتقال حرارت نیز همانند انرژی است. انتقال حرارت با Q نشان داده میشود و این مقدار بر واحد جرم را با q نمایش میدهند.
میزان انتقال حرارت صورت گرفته بر واحد زمان را نرخ انتقال حرارت مینامند. به فرآیندی که در آن هیچ انتقال حرارتی اتفاق نمیافتد، «آدیاباتیک» میگویند.
دانلود جزوه ترمودینامیک 1 | 20 میشم

دانلود جزوه ترمودینامیک 1 | 20 میشم
کار
انرژی که به دلیل اختلاف فشار و یا نیرو به سیستم وارد و یا از آن خارج میشود را کار مینماند و آن را با W نشان میدهند.
کار شفت، انرژی مکانیکی است که محور دستگاههایی همچون پمپ، توربین و یا کمپرسور را به چرخش در میآورد.
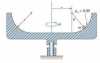
به میزان انرژی انتقال یافته بر واحد زمان، توان گفته میشود. میتوان جهت جریان ورودی و یا خروجی از سیستم را در معادلات مربوطه با in و out نشان داد. در شکل زیر میتوانید شماتیکی از مبادله انواع انرژی با سیستم را مشاهده کنید.
مطلب مرتبط :
حل المسائل ترمودینامیک ون وایلن
دانلود جزوه ابزار دقیق پیشرفته
دانلود جزوه انتقال حرارت هسته ای
قانون اول ترمودینامیک
قانون اول ترمودینامیک، بر مبنای آزمایشات صورت گرفته، بیان میکند که انرژی نه میتواند به وجود بیاید و نه از بین برود بلکه از شکلی به شکل دیگر تبدیل میشود. بر مبنای این قانون، تغییرات انرژی کل یک سیستم را میتوان به صورت زیر بیان کرد:
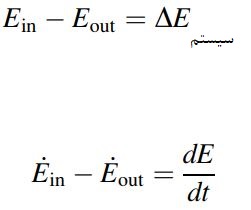
برای سیستم بستهای که تحت یک فرآیند از حالت 1 به 2 تغییر میکند، میتوان نوشت:
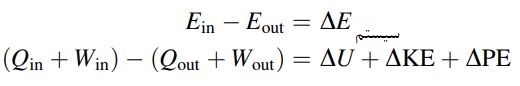
با فرض ثابت بودن انرژی پتانسیل و جنبشی، رابطه زیر برقرار است:
![]()
حال سیستمی را در نظر بگیرید که یک فرآیند پایا را تجربه میکند. در چنین فرآیندی، انرژی و جرم کلی سیستم ثابت است؛ بنابراین قانون اول ترمودینامیک، برای این سیستم به صورت زیر است:
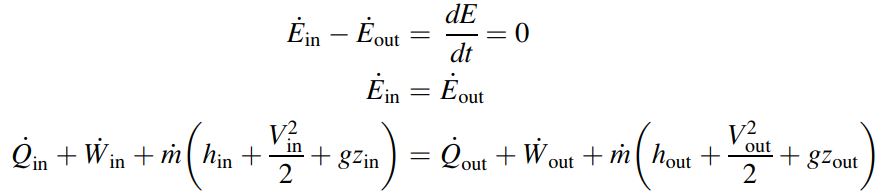
با صرف نظر کردن از تغییرات انرژی جنبشی و پتانسیل میتوان نوشت:
![]()
به عنوان مثال، فرآیند پر و یا خالی کردن یک مخزن از گاز را در نظر بگیرید. توجه داشته باشید که در اکثر فرآیندهای ترمودینامیکی، از فرض گاز ایدهآل استفاده میشود. چنین فرآیندی گذرا است؛ بنابراین با در نظر گرفتن جریان به صورت یکنواخت، معادله تعادل انرژی و جرم، به صورت زیر است:
![]()
دانلود جزوه ترمودینامیک 1 | 20 میشم
قانون دوم ترمودینامیک
انرژی پایسته است و تاکنون هیچ آزمایشی این مفهوم را نقض نکرده.
با این حال به منظور اتفاق افتادن یک فرآیند، علاوه بر قانون اول، مفهوم دیگری نیز بایستی صادق باشد. ممکن است این سوال برایتان پیش آمده باشد که چرا با گذشت زمان پیر میشویم؟
یا این که چرا به منظور جلوگیری از فاسد شدن گوشت، بایستی آن را سرد نگه داشت؟ و به طور کلی چرا همواره یک فرآیند، فقط در یک جهت اتفاق میافتد؟
به عنوان مثال، همه ما میدانیم که رها کردن یک فنجان قهوه داغ در اتاق، باعث سرد شدن آن خواهد شد.
این فرآیند، قانون اول ترمودینامیک را تایید میکند، چرا که میزان انرژی که قهوه از دست میدهد، معادل است با انرژی که هوای محیط اطرافش دریافت میکند.
حال فرآیندی عکس واقعیت را در نظر بگیرید. فرض کنید که قهوه با گذشت زمان داغتر میشود. همه ما میدانیم که چنین فرآیندی هیچوقت اتفاق نخواهد افتاد؛ فرآیند مفروض قانون اول ترمودینامیک را نقض نخواهد کرد، پس به راستی چرا این فرآیند هرگز در واقعیت رخ نمیدهد؟
راز تمام این پدیدهها در قانون دوم ترمودینامیک نهفته است.
در ادامه بیشتر در مورد این قانون صحبت خواهیم کرد. همواره و در هر حالت، به منظور اتفاق افتادن یک فرآیند، هم قانون اول ترمودینامیک و هم قانون دوم، نباید نقض شوند.
دانلود جزوه ترمودینامیک 1 | 20 میشم
در ادامه نشان خواهیم داد که اتفاق افتادن یک فرآیند با خاصیتی ترمودینامیکی به نام «آنتروپی» (Entropy)، مرتبط است. قانون دوم، نه تنها به ما نشان میدهد که یک فرآیند، در یک جهت خاص اتفاق میافتد بلکه به ما یادآور می شود که علاوه بر کمیت، کیفیت نیز برای انرژی قابل تعریف است.
تفاسیر بسیاری از قانون دوم ترمودینامیک مطرح شده؛ شناخته شدهترین نظرات در مورد این قانون، توسط «پلانک» (Planck)، «کلوین» (Kelvin) و «کلازیوس» (Clausius) ارائه شده است.
بیان کلوین-پلانک میگوید: «ساخت دستگاهی که تنها هدف آن، دریافت حرارت از یک منبع و تبدیل تمامی آن، به کار خالص باشد، غیرممکن است.» کلازیوس نیز قانون دوم را از دیدگاه خود به این صورت تفسیر میکند: «هیچگاه نمیتوان دستگاهی ساخت که تنها هدف آن، انتقال حرارت از منبع دما پایین به منبع دما بالا باشد.»
دانلود جزوه کامل درس ترمودینامیک
دانلود جزوه ترمودینامیک 1 | 20 میشم

دانلود جزوه ترمودینامیک 1 | 20 میشم
آنتروپی
غالبا مباحث مربوط به قانون دوم ترمودینامیک در مورد کیفیت کار انجام شده و پتانسیل تبدیل انرژی به کار، صحبت میکند.
به عنوان نمونه این قانون بیان میکند، موتور حرارتی که در یک سیکل برگشت پذیر کار میکند از راندمان بالاتری برخوردار است؛ این همان مفهومی است که قبل از کشف این قانون، توسط «سعدی کارنو» (Saadi carnot) و در قالب «راندمان کارنو» به آن پرداخته شده بود.
ولین بار «کلازیوس» (Clausius)، دانشمند آلمانی بود که مفهوم قانون دوم ترمودینامیک را در قالب ریاضیات و به صورت زیر بیان کرد:
![]()
این معادله، بیان میکند که همواره انتگرال انتقال حرارت بر دمای سیستم، در یک سیکل بسته، کمتر و یا مساوی صفر است. کلازیوس در سال 1865 متوجه شد که خاصیت جدیدی را در ترمودینامیک کشف کرده . او این خاصیت را آنتروپی نامید که با S نشان داده میشود. ازدیاد آنتروپی همان فرآیندی است که منجر به پیری میشود. هم چنین این ازدیاد، باعث فاسد شدن گوشت و یا خراب شدن یک میوه پس از گذشت مدت زمان معینی میشود. تغییرات جزئی آنتروپی برابر است با:
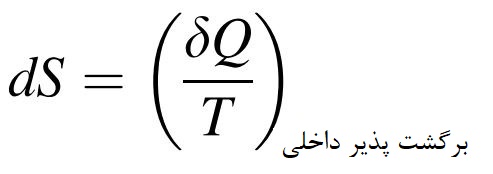
در حقیقت آنتروپی یک خاصیت مطلق در ترمودینامیک است؛ گاهی از آن با عنوان «آنتروپی مطلق» (Total entropy)، یاد میشود. آنتروپی بر واحد جرم را با s نشان میدهند که یک خاصیت مقداری است. تغییرات آنتروپی یک سیستم، که طی یک فرآیند، تغییر حالت می دهد را میتوان با انتگرال گیری از معادله بالا و به صورت زیر محاسبه کرد:
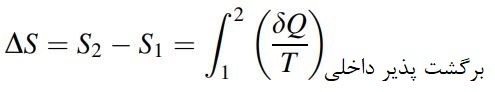
توجه شود که آنتروپی یک خاصیت است، بنابراین در هر حالتی که سیستم قرار گرفته باشد، میتوان یک مقدار از آنتروپی را به آن نسبت داد. در نتیجه، تغییرات آنتروپی برای یک سیستم، که از حالت 1 به 2 تغییر میکند، ثابت است و وابسته به مسیر فرآیند نیست.
حال چرخهای را در نظر بگیرید. این چرخه را میتوان به صورت دو فرآیند در نظر گرفت که در آن سیستم از حالت 1 به 2 میرود و دوباره از حالت 2 به 1 برمیگردد. فرآیند 1 به 2 در این چرخه، میتواند برگشت پذیر و یا برگشت ناپذیر باشد؛ فرآیند دوم نیز به صورت درونی، برگشت پذیر در نظر گرفته شده. نامساوی کلازیوس برای چرخه مفروض به شکل زیر است:
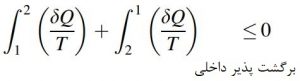
عبارت اول در معادله بالا همان تغییرات آنتروپی از حالت 1 به 2 است. بنابراین میتوان در ادامه نوشت:
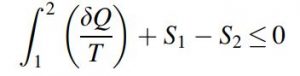
این معادله را میتوان به صورت زیر مرتب کرد:
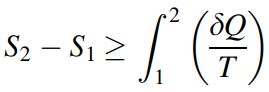
این معادله بیان میکند که آنتروپی کل تولید شده در تمامی فرآیندها همواره بیشتر از آنتروپی منتقل شده است.
به منظور فهم بیشتر موضوع، اجازه دهید مثالی بزنیم. فرض کنید یک فنجان قهوه در اتاقی با دمای 25 درجه قرار گرفته است. کاملا بدیهی است که پس از مدتی این فنجان قهوه سرد خواهد شد.
بنابراین آنتروپی خود قهوه، کاهش و آنتروپی اتاق، افزایش مییابد؛ این در حالی است که آنتروپی کل سیستم (قهوه + محیط اطراف) افزایش یافته است.
دانلود جزوه ترمودینامیک 1 | 20 میشم
دانلود جزوه انتقال حرارت هسته ای
دانلود جزوه فصل اول ترمودینامیک 1
فرمول های ترمودینامیک
فهرست سرفصل ها
- درس یکم: توضیحات مقدماتی
- نیروگاه ساده بخاری
- پیل های سوختی
- سیکل تبرید تراکم بخار
- یخچال ترموالکتریکی
- جداساز هوا
- توربین گازی
- موتور موشکی شیمیایی
- دانلود جزوه ترمودینامیک 1 | 20 میشم
- درس دوم: مفاهیم و تعاریف اولیه
- سیستم، جرم کنترل و حجم کنترل
- خواص و حالت یک ماده
- خواص و سیکل ها
- آحاد ترمودینامیکی
- انرژی
- خواص در واحد جرم
- فشار
- قانون صفرم ترمودینامیک
- مقیاس های دما
- درس سوم: خواص ماده خالص
- ماده خالص
- تعادل فازها
- خواص مستقل ماده خالص
- معرفی و کاربرد جداول ترمودینامیکی
- سطوح ترمودینامیکی
- رفتار گازهای ایده آل و غیر ایده آل
- درس چهارم: کار و گرما
- تعریف کار و آحاد آن
- کار انجام شده در مرز متحرک سیستم
- انواع کار
- تعریف گرما
- انواع انتقال گرما
- مقایسه کار و گرما
- دانلود جزوه ترمودینامیک 1 | 20 میشم
- درس پنجم: قانون اول ترمودینامیک
- تعریف قانون اول ترمودینامیک، در جرم کنترل
- تعریف قانون اول ترمودینامیک برای تغییر حالت در جرم کنترل
- انرژی درونی
- تحلیل مسائل و روش حل مسائل ترمودینامیکی برای جرم کنترل
- آنتالپی
- تعریف گرمای ویژه در حجم ثابت و فشار ثابت
- تعریف آنتاپی و ظرفیت های گرمایی گازهای ایده آل
- بیان قانون اول ترمودینامیک به صورت آهنگی
- درس ششم: تحلیل قانون اول ترمودینامیک برای حجم کنترل
- حجم کنترل و پایستاری جرم
- تعریف قانون اول ترمودینامیک برای حجم کنترل
- فرایندهای پایا و کاربردهای آن ها
- فرایندهای گذرا و کاربردهای آن ها
- درس هفتم: قانون دوم ترمودینامیک
- ماشین های گرمایی و یخچال ها
- بیان قانون دوم ترمودینامیک
- فرایند برگشت پذیر
- عواملی که باعث برگشت پذیر نشدن فرایندها می شوند
- سیکل کارنو (Carnot cycle) و نکات مربوط به بازده
- مقایسه ماشین های ایده آل و واقعی
- درس هشتم: آنتروپی
- نامساوی کلازیوس (Clausius)
- آنتروپی
- تغییر آنتروپی در فرایندهای برگشت پذیر
- رابطه های خواص ترمودینامیکی
- تغییر آنتروپی جرم کنترل در فرایند برگشت ناپذیر
- تولید آنتروپی و اصل افزایش آنتروپی
- تغییر آنتروپی جامدات و مایعات و گازهای ایده آل
- فرایند پلی تروپیک (Polytropic)
- معادله آهنگی آنتروپی
- درس نهم: تحلیل قانون دوم ترمودینامیک در حجم کنترل
- قانون دوم ترمودینامیک برای حجم کنترل
- فرایند پایا و گذرا با در نظر گرفتن قانون دوم ترمودینامیک
- فرایند برگشت پذیر پایا
- اصل افزایش آنتروپی
- بازده
دانلود جزوه ترمودینامیک 1 | 20 میشم
یکی از کاربردهای مهم و هیجانانگیز علم ترمودینامیک، در سیستم های بیولوژیکی (Biological Systems) است. سیستم های بیولوژیکی محل وقوع پدیدههای تبدیل و انتقال پیچیده انرژی هستند.
این سیستمها در تعادل ترمودینامیکی قرار ندارند.
از این رو، تحلیل آنها کار دشواریست. در کنار این پیچیدگیها، سیستمهای بیولوژیکی را میتوان متشکل از چهار عنصر مختلف به حساب آورد: هیدروژن، اکسیژن، کربن و نیتروژن. در بدن انسان، هیدروژن 63 درصد، اکسیژن 25.5 درصد، کربن 9.5 درصد و نیتروژن هم 1.4 درصد از کل اتمها را شامل میشوند.
باقیمانده اتمها که در حدود 0.6 درصد است، بیست عنصر مختلف را در برمیگیرند که وجودشان برای بدن حیاتی است. از نظر جرمی نیز، در حدود 72 درصد از کل بدن را آب تشکیل میدهد.
دانلود جزوه ترمودینامیک 1 | 20 میشم
دانلود جزوه فصل اول ترمودینامیک 1
فرمول های ترمودینامیک

دانلود جزوه ترمودینامیک 1 | 20 میشم
تعریف متابولیسم در سیستم های بیولوژیکی
بلوکهای ساختمانی هر ارگانیزم زنده، سلول نامیده میشود.
سلولها در نقش کارخانههای مینیاتوری، وظایفی را به عهده دارند که برای زنده ماندن هر ارگانیزم ضروری است.
سیستم های بیولوژیکی میتوانند به سادگی یک سلول باشند. بدن انسان از حدود یکصد تریلیون سلول تشکیل شده که قطر متوسط این سلولها در حدود 0.01 میلیمتر است.
دانلود جزوه ترمودینامیک 1 | 20 میشم
غشای سلول، از یک دیواره شبهنفوذپذیر (Semipermeable) تشکیل شده که به برخی مواد اجازه ورود میدهد و از عبور برخی مواد دیگر جلوگیری میکند.
در سیستم های بیولوژیکی در هر ثانیه، درون هر سلول هزاران واکنش شیمیایی در حال وقوع است.
در حین هر واکنش شیمیایی، برخی مولکولها تجزیه شده و انرژی آزاد میشود. در ادامه این روند، برخی مولکولهای جدید هم تشکیل میشوند.
تمام واکنشهای شیمیایی در حالی رخ میدهند که دمای بدن انسان، در 37 درجه سلسیوس ثابت مانده است. این حجم از فعالیتهای شیمیایی درون سلولها، که برای انجام وظایف اصلی بدن رخ میدهد، متابولیسم (Metabolism) نامیده میشود.
به عبارت ساده، متابولیسم را میتوان به عنوان سوختن مواد غذایی مانند کربوهیدراتها، چربیها و پروتئینها در سیستم های بیولوژیکی تعریف کرد.
نرخ متابولیسم در حالت استراحت، نرخ متابولیک پایه (Basal Metabolic Rate) نامیده میشود.

دانلود جزوه ترمودینامیک 1
دانلود جزوه ترمودینامیک 1 | 20 میشم
نرخ متابولیک پایه که به اختصار، BMR نیز خوانده میشود، عبارت است از نرخ متابولیسم لازم برای انجام کارهای ضروری بدن، هنگامی که سطح فعالیت خارجی برابر صفر است.
تنفس و خونرسانی جزء کارهای ضروری محسوب میشوند. از طرف دیگر، نرخ متابولیک را میتوان به عنوان نرخ مصرف انرژی بدن توصیف کرد. در یک مرد متوسط، نرخ متابولیک پایه برابر 84W است.
مردی با 30 سال سن و 70kg وزن که مساحت بدنش برابر 1.8m2 باشد را به عنوان مرد متوسط تعریف میکنیم.
در واقع، بدن چنین فردی، با نرخ 84W انرژی را به محیط منتشر میکند. به عبارت دیگر، تبدیل انرژی شیمیایی موجود در مواد غذایی (یا چربی بدن) به انرژی گرمایی با نرخ 84W در حال انجام است.
دانلود جزوه ترمودینامیک 1 | 20 میشم
دانلود جزوه فصل اول ترمودینامیک 1
فرمول های ترمودینامیک
توضیحات تکمیلی
بدون شک یکی از مهم ترین و اساسی ترین دروس تحصیلات تکمیلی برق قدرت، درس دینامیک سیستم های قدرت می باشد.
دینامیک سیستم های قدرت به درک، مدل سازی، تحلیل و روش های بهبود مسائل کنترل و پایداری در سیستم های قدرت می پردازد.
از زمان پیدایش سیستم قدرت، هر چه از عمر این صنعت گذشته، وسعت این سیستم در اثر متصل سازی شبکه ها، پیچیده تر و بزرگ تر شده است و به همان اندازه تجزیه و تحلیل آن دشوارتر گردیده است.
دانلود جزوه ترمودینامیک 1 | 20 میشم
در این میان، قیود مالی و مقررات، شرکت های برق را مجبور به استفاده از سیستم ها در مرز پایداری خود کرده اند.
هدف اصلی در یک سیستم قدرت، تحویل توان لازم مصرف کننده در ولتاژ و فرکانس مشخص است.
همین امر منجر شده تا مسأله طراحی کنترل کننده و نظارت دقیق اپراتورها بیش از پیش جلب توجه کند.
در همین راستا باید گفت که انجام نظارت و طراحی کنترل کننده مناسب بدون انجام مطالعات دینامیکی کافی، نتیجه لازم را نخواهد داد. دینامیک سیستم های قدرت به منظور آشنایی دانشجویان و مهندسان برق صنعتی با مفاهیم دینامیک و کنترل سیستم های قدرت بنا شده است.
توجه : فایل دانلود PDF مجموعه فرمول های ترمودینامیک ۱ و ۲ کنکور کارشناسی ارشد مهندسی شیمی در تاریخ اول بهمن ماه 1401 بصورت رایگان به این مجموعه دانلودی اضافه شد .


از این که تا پایان متن با ما همراه بودید سپاسگزاریم.
دانلود جزوه کامل درس ترمودینامیک
دانلود جزوه فصل اول ترمودینامیک 1
فرمول های ترمودینامیک
منبع:گوگل
ترمودینامیک,تعادل ترمودینامیکی,جزوه ترمودینامیک 1,دانلود جزوه ترمودینامیک 1,دانلود جزوه فصل اول ترمودینامیک 1,فرمول های ترمودینامیک
درباره این محصول نظر دهید !
- توضیحات محصول را به خوبی بخوانید و در صورت نیاز به راهنمایی از بخش کاربری و سیستم تیکت استفاده نمایید .
- پشتیبانی محصولات سیستم تیکت و تماس از طریق واتس آپ می باشد .
- برای دریافت آخرین نسخه محصولات و دسترسی همیشگی به محصولات خریداری شده حتما در سایت عضو شوید .
- پرداخت از طریق درگاه بانکی انجام میشود در غیر این صورت با ما تماس بگیرید